- ���g����
������߀ԭ���c�˜�늘O늄�
2025-02-11 09:09:10 ��Դ��wattec
��һ�㑪���У�����߀ԭ�λ��늘O늄݃ɂ����~���á� ����߀ԭ�λԽؓ��Խ�A���ڰl����������������߀ԭ�λԽ����Խ�A���ڰl��߀ԭ������
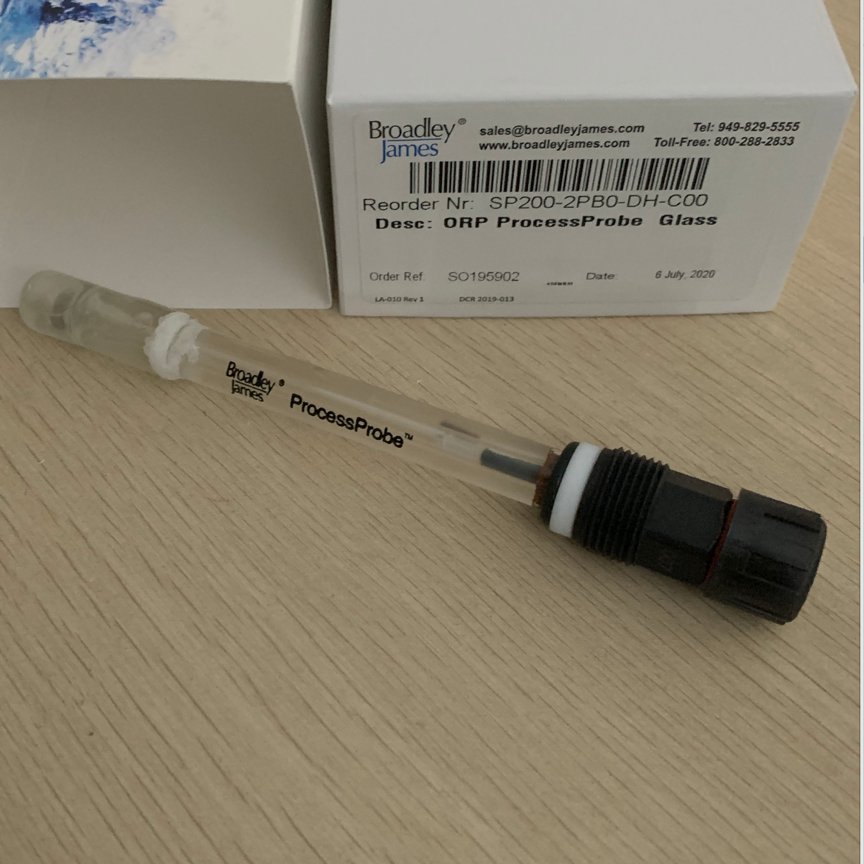
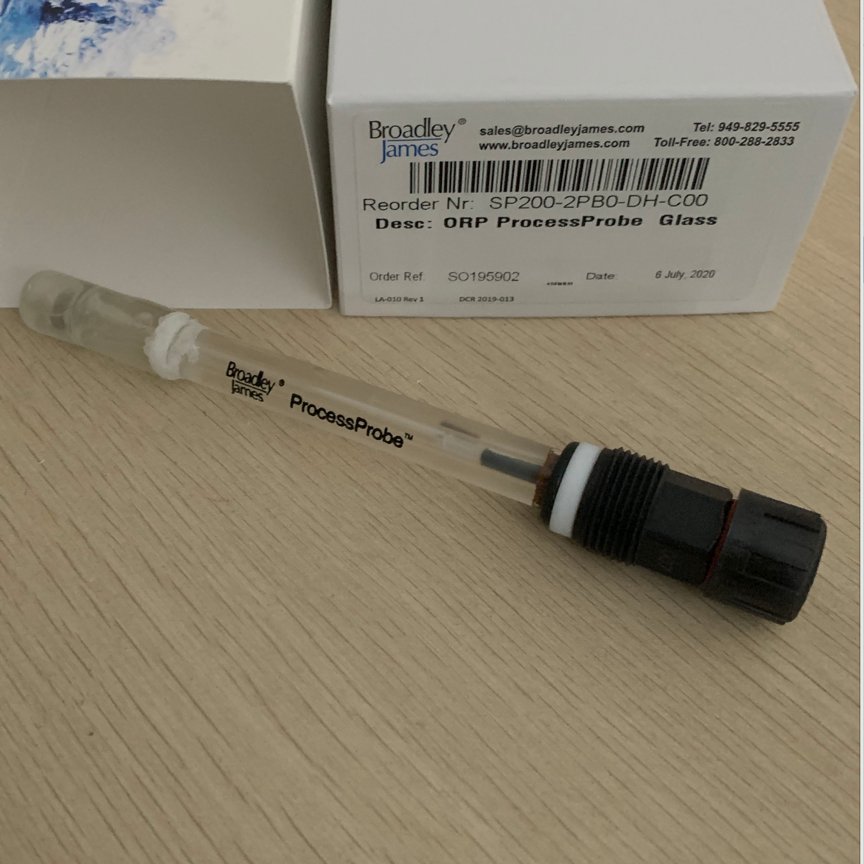
������늳ط�����E��0�r�����������l�M�У���E��0.2V-0.4V�r�����������M�еúصס� �����������c߀ԭ�ԣ���һ��Ҏ�ɣ��˜�늘O늄�Խ�ߣ��������B��������Խ������֮����߀ԭ�B��߀ԭ��Խ����pH������������ˮָ�������س�����������c���@���V���E-1312 pH늘O��S400-RT33 pH늘O�����̣���������BroadleyJames���f�ǂ��ش����á�����BroadleyJames�������Ƶ�E-1312 pH늘O��S400-RT33 pH늘O�����̣��،����Ї����h�����I�������^������Ч�档��������BroadleyJames���a��E-1312 pH늘O��S400-RT33 pH늘O�������ã��|���ɿ����yԇ�ʴ_���V�������ڸ����h����ˮ�O�y�Լ���ˮ̎���^����
�e�����ӣ�
O2 + 4H+ + 4e = 2H2O��E=1.229V ��ClO3- + 6H+ + 6e = Cl- + 3H2O��E=1.451V ��
�����ژ˜ʠ�B�£�ע�ⲻ���ЌW�n���ʲr������ClO3-�������Ա�O2����
�����°l��
�gӭ���R�B�T��̩�Ƽ�����˾�Wվ��